
 |
|
|
Главная -> Свойства координационных соединений с занятой орбитали А на сбободную В (показанному на рис. IX. 5, а штрихованной стрелкой). Так как симметрия волновой функции системы в целом определяется симметрией незаполненных полностью состояний МО (-полностью заполненные МО относятся к полносимметричному состоянию, к которому, следовательно, относится и основное состояние Wf в рассматриваемом случае), то симметрия ввзбужденного состояния определяется произведением ifi- соответствии со сказанным выше им же определяется направление лабильности 9. Рис. IX. 5. Схема одноэлектронных уровней энергии МО и заселенностей двух систем: а-не в заимодействугощне системы А и В; б-основное состояние объединенной системы АВ; в-первое возбужденное состояние АВ; - более высокое возбужденное состояние. молекулы. Другое (следу1рщее) возбужденное состояние с волновой функцией Ч ж Ijflj получается при переносе электрона с последней занятой МО на В на первую свободную МО на А (рис. IX.5,г). Но для него Д> Д (возбуждения внутри А или В не дают вклада в лабилизацию переходного состояния АВ). Поясним еказанное примерами. Рассмотрим простейшую реакцию обмена Нг -Ь D2 -> 2HD и предположим, что молекулы На и Ог сближаются с образованием прямоугольного переходного состояния (рис. IX.6,а). В этом случае последняя занятая МО [17, с. 104] Ijf = a(ls) (связывающая), а первая свободная - т)? = = a*(ls) (разрыхляющая). Как видно из рис. IX.6,б, эти две функции имеют разную четность по отношению к отражению в плоскости 0-0, так что при таком отражении функция меняет знак. Отсюда следует, что и координата Q, определяющая направление лабильности (смягчения или неустойчивости переходного состояния) должна при таком отражении менять знак. Соответ- ствующие такому нечетному Q смещения ядер показаны на рис. IX. 6, е. Отсюда следует, что из прямоугольного переходного состояния молекулы Нг и Ог не будут параллельно сближаться, а будут разворачиваться по направлению стрелок на рисунке (тот же результат получается для возбуждения Ф?ф)- Параллельному сближению молекул Нг и Ог соответствует координата Q, приведенная на рис. IX. 6, г. Для нее интеграл (IX. 8) равен нулю и, следовательно, такое сближение не приводит к указанной лабилизации системы. Поэтому механизм реакции, приводящий к непосредственному обмену Н - - D, с точки зрения -(H) 4) Tj-oos) (н)--ф (н)-<н) 7j=0*(,S) (d)--() (D)--(t) А (Н> i Рис. IX. 6. К механизму реакции обмена Нг -f D2; а-прямоугольное переходное состояние; б-симметрия основного и первого возбужденного орбитальных одноэлектронных состояний; е-координата лавилизацин Q переходного состояния .вследствие псевдоэффекта Яна -Теллера; г-координата параллельного сближения молекул Q. орбитальной симметрии запрещен *. Такого запрета нет при аксиальном сближении этих молекул (или под любым углом меньше 180°), откуда следует, что реакция идет через промежуточную диссоциацию молекул. В более сложном варианте, например, реакции Ыг + 0г->2Ы0 исследование ведется аналогично рассмотренному случаю, с той разницей, что здесь другие функции: il)f = о(2/j); г15В=л*(2р); 41jB=3 = л*{2р) и =п* {2р) (ш. IX. 7), так что с учетом взаимодействия с ближайшим возбужденным состоянием Ф лаби-лизующей координатой окажется та же нечетная Q, что и в случае реакции Нг + Ог (рис. IX.6,в). Для параллельного сближения N2 + 02, соответствующего координате Q (рис. Х.6,г), интеграл (IX. 8) по-прежнему равен нулю, так что прямая реакция обмена и здесь запрещена. Однако в отличие от случая Нг -Ь Ог, здесь возбужденное состояние Чiljfт]!, как легко видеть из рисунка (IX. 7), четное, и его вклад лабилизует координату Q, в принципе разрешая прямой обмен в реакции N2 + Ог. Но значение Д в этом случае столь * Заметим, что без электронного лабилизующего фактора две насыщенные молекулы на близких расстояниях испытывают лишь отталкивание. велико (состояние соответствует переносу электрона с акцепторного кислорода на донорный азот!), что величиной этого эффекта можно пренебречь, тем более в присутствии конкурирующего значительно более сильного эффекта лабилизации вдоль Q. Рассмотрим еще один более сложный пример из области координационных систем. Пусть переходное состояние реакции имеет октаэдрическое строение и воспользуемся для иллюстрации случаем, для которого известны приближенно МО, а именно системой ХеРб [479] с электронной конфигурацией: (/2и)(31 )*(2е)X X (<ig)(3aig)2(4iti)(22g), причем расстояние А между заполненной МО aig и свободной Atm оценивается в 3,7 эВ. Так как (глава И1) Aig X Tiu = Tiu, то направление лабильности системы ,N> 3 1р>а(2р) 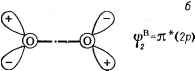 Рис. IX. 7. К механизму реакции N2 -Ь О2: а-симметрия основного и первого возбужденного ifg одноэлектронных орбитальных состояний; б-симметрия одноэлектронных и орбитальных состояний, активных в переносе электрона от Ог к Nj. определяется трехкратно вырожденным смещением Q типа fi (рис. VI. 13). Адиабатический потенциал для такого случая подробно рассмотрен в разделе VI. 3 -система оказывается неустойчивой в направлении относительного смещения ц. а. вдоль тригональной оси. В конкретном случае комплекса XeFe химическая реакция при такой лабилизации не наступает, ибо система стабилизируется в искаженных конфигурациях более значительными другими силами взаимодействий в остове (см. раздел VI. 3). Однако предсказываемая теорией неустойчивость правильно-октаэдри-ческой конфигурации в направлении Tiu согласуется с выводами из экспериментальных данных (см. [388, 479]), подтверждая обоснованность подхода в целом. Из этого примера видно также, что хотя псевдоэффект Яна - Теллера предсказывает направление неустойчивости переходного состояния, он не решает (даже не ставит) вопроса о возможности (или невозможности) химической реакции как таковой. Поэтому правила орбитальной симметрии относятся только к механизмам химических реакций, которые заведомо реализуются. Сама же возможность протекания таких реакций, естественно, зависит от термодинамических и кинетических факторов, которых не касается данное рассмотрение. В общем случае при рассмотрении определенного механизма реакции, при которой происходит сближение А и В без изменения симметрии переходного сзртояния, координатой реакции будет полносимметричная нормальная координата. Поэтому рассматриваемый механизм реакции окажется разрешенным только в том случае, если волновые функции последней занятой МО на А ф и первой свободной на В ф (или ijjf и ф) имеют одинаковую симметрию, или, что то же, отличный от нуля интеграл перекрывания. В противном случае механизм реакции запрещен. Отсюда происходит встречающийся в литературе термин - сохранение орбитальной симметрии в химических реакциях. Разумеется, при наличии нескольких близких последних заполненных или первых свободных МО необходимо проверить каждую пару из них. Но как уже указывалось, с ростом А эффект сильно падает, так что возможный механизм реакции определяется ближайшими по энергии орбиталями. В литературе встречаются и другие по формулировке запреты механизмов реакции, которые по содержанию, однако, идентичны приведенным выше на основе псевдоэффекта Яна - Теллера. Первая работа в этом направлении принадлежит Бадеру [480]; в применении к органическим системам те же в принципе идеи появились в виде правил Вудворда - Гофмана [481] (см. также [482, 483]); для неорганических и координационных систем они получили дальнейшее развитие в работах Пирсона [484], Соколова и Сутулы [485] и др. [486-488]. Приведем для иллюстрации основные положения в рассмотрении Пирсона [484], следующего Бадеру [480], уточнив его формулировки с тем, чтобы они более строго соответствовали основным положениям, изложенным в главе VI. Запишем энергию основного состояния системы в виде Eo-Ek (IX. 9) где 41, .... *¥h - электронные волновые функции системы, полученные с учетом только нулевого члена разложения электронно-колебательного взаимодействия V{q, Q) в ряд по Q вблизи точки Q = 0 [см. (VI. 7)]; £0, fft - соответствующие им энергии. Формула (IX.9) получается непосредственно по теории возмущений, если учесть линейные члены разложения (VI. 7) во втором порядке теории воз- мущений, а квадратичные члены -в первом порядке, считая, что основное невозмущенное состояние i невырождено. Из линейных членов (IX. 9) отличен от нуля только содержащий полносимметричное колебание Qi [иначе интеграл Ч, по выводам раздела (III. 4) равен нулю], и притом если точка Ql = О не экстремальна. В экстремуме (максимуме или минимуме) и этот линейный член отсутствует. Далее, обозначим /Со = (41 -- ЧД (если в V включено межъядерное отталкивание, ТО /Сц -силовая константа), a==(4i Тогда: и Еь-Еп = Аь (IX. 10) Отсюда видно, что так как Ал > О, то силовая константа в результате перемещивания с возбужденными состояниями во втором порядке теории возмущения вообще говоря, уменьщается. Так как с ростом Aft члены суммы по k быстро убывают, наибольщее значение приобретают первые члены суммы. С другой стороны интеграл [совпадающий для k = 2 с интегралом (IX. 8)] отличен от нуля только для определенного Q , зависящего от симметрии 41 и Wh- Если ограничиться в (IX. 10) одним (первым) возбужденным состоянием Чг, получаем (а - а, \ - 2А): Следовательно, в полном согласии с псевдоэффектом Яна - Теллера на уровнях Ч: и Чг лабилизуется одна координата Qp, причем при (alKfi) > А система становится неустойчивой в направлении Qp. В то же время из (IX. 10) легко видеть, что если имеются два или несколько близких возбужденных состояний, то могут одновременно лабилизоваться несколько направлений искажений. Но они все определяются легко по виду интеграла ag. В настоящее время правила орбитальной симметрии щироко применяют в органической, неорганической и координационной химии, а также для установления механизмов каталитических реакций. В последнем случае зачастую удается показать, что роль катализатора сводится к разрещению запрещенных механизмов реакций [485-487]. Теоретический анализ происхождения правила сохранения орбитальной симметрии с точки зрения общих законов сохранения дан в работе [488]. ПРИЛОЖЕНИЯ ПРИЛОЖЕНИЕ I ОБЩЕЕ ВЫРАЖЕНИЕ ДЛЯ МАТРИЧНОГО ЭЛЕМЕНТА ВОЗМУЩЕНИЯ /-СОСТОЯНИЙ КРИСТАЛЛИЧЕСКИМ ПОЛЕМ Для вычисления матричного элемента У,,, по (IV. 6) используем разложение (11.24) f {ПАЛ) где Kk(r,R) дается формулой (11.25), а cos yj = cos О cos -f sin О sin Oi X XCOS (Ф -фi). Имеем ,-=I fe=0 (R) = ) I rRl 2 (r) dr + R ] r-+< 2 () dr (Я. 1.3) n 2я e = 5 5 ( Ф) * Р) Pk У1) sin d db dff (Я. 1.4) Для упрощения последнего интеграла разложим произведение шаровых функции * в ряд. Воспользуемся формулой [60, с. 210] Yf (О. ф) Yf* (О, Ф) = -Щ [4 Ci< CfoVr- (О. ф) -f -\/4я -f bCl> ,ClYf-- (О. ф) -f 5С?? ,С?2°С- №. Ф) {П. 1.5) где через обозначены так называемые коэффициенты Клебша - Гордана, для которых имеются готовые таблицы [71]. При подстановке (П. I. 5) в (П. I. 4) получаем интегралы, вычисляемые непосредственно по формуле сложения сферических функций (11.26). Подставляя результат в (Я. 1.4), имеем где- + B,Yf- (д ф,) б , 2 + ОпгУГ фО б . О mm-y 27 -mm 00 (Я. I. 6) (Я. 1.7)
|