
 |
|
|
Главная -> Свойства координационных соединений в табл. IX. 1 приведены экспериментальные кинетические данные для диссоциации (реакция 5jvl) некоторых о-фенантролино-вых и а,а-дипиридиловых комплексов переходных металлов при 25 °С [446] и теоретические данные для изменения энергии экстрастабилизации в предположении, что промежуточное состояние является квадратной пирамидой. Значения энергии получены с помощью данных табл. IV. 10 и IV. 11 в единицах параметра расцепления Д и переведены в кДж/моль (ккал/моль) с учетом соотношения Д л; 167,6 кДж/моль ( 40 ккал/моль), получаемого из спектральных данных для этих соединений. Мы видим, что в пределах приближенности оценок изменения энергий экстрастабилизации находятся в некотором относительном согласии с экспериментально определенными энергиями активации (в том смысле, что увеличение энергии экстрастабилизации пропорционально наблюдаемому увеличению высоты барьера реакции). В то же время легко заметить, что это согласие довольно грубое, неточное, так что с учетом только изменения энергии экстрастабилизации нельзя получить надежных сведений о ходе реакции. Для реакций типа 5jv2 большую, чем изменение энергии экстрастабилизации, роль может играть изменение взаимного отталкивания лигандов. Дело в том, что само сближение внешнего реагента, достаточное для его вступления в непосредственную связь с металлом, определяется в первую очередь факторами его отталкивания от лигандов. Вполне понятно, что при этом наряду с размерами последних большое значение имеет зарядовое распределение на них. Нуклеофильному замещению препятствует отрицательный и способствует положительный заряд, электрофильному - наоборот. Поэтому распределение заряда в исходном комплексе часто играет определяющую роль и оказывается непосредственным показателем реакционной способности. Зарядовое распределение существенно также для реакции 5jvl (ср. с зависимостью кислотных свойств лигандов от эффективного заряда на центральном атоме). Оно может оказаться эффективной характеристикой реакционной способности и в более сложных случаях (например, возможность образования двуядерного алканоата меди зависит от эффективного заряда монокарбоновых кислотных остатков в соединении [198])*. Поэтому его определение является важной задачей координационной химии. Для определения зарядового распределения в системе можно воспользоваться методом МО ЛКАО (гл. V), например, в форме полуэмпирического варианта МВГ, включающего самосогласование зарядов на атомах (стр. 149). В настоящее время известно уже немало работ, посвященных таким расчетам (см. раздел V. 4). Экспериментальное определение зар.чдов встречает известные трудности. Прямых и практически удобных методов его определения почти нет. Трудности встречаются уже при определении понятия заряда части соединения, например, эффективного заряда на атомах. При расчетах по методу МО ЛКАО это понятие имеет определенный математически четко определяемый смысл. Однако в экспериментах проявляется несколько другой заряд, причем в разных экспериментах разные заряды, и не всегда ясно, с чем нужно эти заряды сравнивать, чему их приписать. Эти трудности относятся и к рентгеноспектральному методу определения эффективных зарядов на атомах, хотя, конечно, ряд качественных выводов о зарядовом распределении на основе этих методов можно получить (см. раздел VII. 5). Взаимное влияние лигандов. транс- и цис-влияние С точки зрения сказанного выше вполне естественно, что реакция замещения данного лиганда в координационном соединении зависит как от природы центрального атома, так и от природы остальных лигандов. Познание характера этих зависимостей очень важно как в теоретическом, так и в практическом плане. Первая, весьма четкая, закономерность такого рода была впервые установлена И. И. Черняевым в 1926 г. и получила название транс-влияния [447]. Сущность этого явления сводится к тому, что скорость реакции замещения данного лиганда определяется главным образом природой лиганда, расположенного в транс-положении к нему. Чем более активным в смысле транс-влияния является данный лиганд, тем больше скорость замещения его транс-партнера в координационном соединении. С учетом транс-влияния возможность замещения лиганда А в комплексе L-М-А определяется в основном природой L, а в комплексе Li-М-А, с большей скоростью произойдет замещение того из лигандов - Ai или Аг, - в транс-положении к которому стоит более активный в смысле транс-влияния лиганд: Li или Ьг. Роль же лигандов В при замещении А или L2 и Аг при замещении Ai второстепенна (см. ниже). Транс-влияние было установлено и затем неоднократно исследовалось на большом числе соединений, главным образом плоскоквадратных двухвалентной платины. В дальнейшем оно было распространено и на октаэдрические комплексы, а также на комплексы других металлов [92, гл. 5; 444, 448-450], хотя в этих случаях оно проявляется менее четко. Из опытных данных вытекает примерно следующий ряд убывания трапс-активкостей атомных групп-лигандов: с2н4, CN-, СО > PRa, Н- > SC(NH2)2 > > no;, SCN > г > Br > CI > f > NH3, En Py, RNH2 > oh- > H2O (IX. 1) Вполне естественно, что наряду с основным транс-влиянием, определяющим место замещения в координационной системе, скорость этого замещения будет зависеть и от цис-лигандов. Именно такой цис-эффект был обнаружен и исследован А. А. Гринбергом с сотрудниками [451]. Оказалось, что в принципе можно установить и ряд цис-влияний на скорость реакции транс-замещения. Однако из-за слабости эффекта (по сравнению с транс-влиянием) и его малой изученности в настоящее время пока такой ряд четко не установлен, хотя отдельные закономерности дискутируются (см. ниже). Как транс-, так и цис-влияние обусловлены электронным строением системы и поэтому могут быть объяснены только с его учетом. Из ранних попыток объяснения транс-влияния можно отметить поляризационную теорию Гринберга [452] и Некрасова [453] и теорию цис-закрепления Сыркина [454]. Однако современный уровень исследования электронного строения может послужить основанием для более глубокого подхода. Достаточно полное исследование электронного строения существующими методами, например, в приближении МО ЛКАО (глава V), позволило быпроанализировать зависимость как энергии связи данного лиганда от его транс-партнера (существенную для исследования замещения по механизму 5jvl), так и распределение электронного облака вдоль системы (существенного при замещении по механизму 52). Такого достаточно полного исследования до сих пор, насколько нам известно, никто не проводил*.- Некоторые качественные аспекты проблемы были рассмотрены Чатом, Данкансоном и Венанци [456] и независимо от них Оргелом [457] и затем продолжены автором [458]. В основе рассмотрения лежит предположение, что реакция нуклеофильного замещения проходит по механизму 5jv2 и что главным фактором, определяющим скорость реакции, является несимметричное зарядовое распределение в исходном комплексе, благодаря которому замещение по координате с меньшей плотностью электронного облака проходит с меньшей энергией активации. С учетом этого предположения возникновение транс-влияния объясняется следующим образом. Рассмотрим плоскоквадратный комплекс Pt(II) и качественно исследуем распределение плотности электронного облака в нем в зависимости от свойств лигандов. Выделим лиганд L, транс- * Расчеты электронного строения некоторых комплексов Pt (II) в этом аспекте см. в работах [455]. 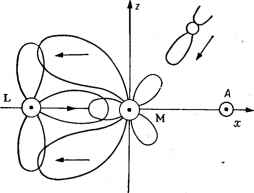 активность которого изучается, п предположим, что он обладает достаточно низколежащими свободными орбиталями, способными к образованию я-связи с центральным атомом. Этих орбиталей нет у остальных лигандов или у них они менее активны. Тогда лиганд L образует дополнительную дативную я-связь, которая приводит к оттягиванию соответствующего я-облака dz- или сгг-орбиты в сторону L. При этом с противоположной стороны вблизи транс-лиганда А освобождается место для входящей группы (либо над, либо под плоскостью комплекса). На рис. IX.3 схематически изображены электронные облака связи в разрезе вдоль координаты L - Pt - А и перпендикулярно к плоскости комплекса. Очевидно, что освобождающееся место для транс-атаки входящей группы естественным образом приводит к трансзамещению. Необходимо подчеркнуть, что в приведенной схеме нигде не предполагается ослабления связи транс-партнера А с центральным атомом. Трансвлияние здесь сводится исключительно к уменьшению энергии активации промежуточного активированного комплекса , приводящего к транс-замещению. Что касается транс-связи, то ее ослабление или усиление в таком ме-ханивме реакции не играет решающей роли *. Таким образом, в теории Чата с сотрудниками и Оргела трансвлиянию группы L ставится в соответствие ее я-акцепторные свойства. Это позволяет объяснить высокую транс-активность таких групп, как С2Н4, CN , СО, NO2 и др. Однако многие активные лиганды не являются я-акцепторамп и не попадают под объясие ние Чата -Оргела. Наоборот, А. А. Гринбергом установлено [459], что для значительного числа случаев наблюдается параллель между транс-активностью и восстановительными свойствами групп. Дополнение к этим представлениям [458], основанное на учете взаимозависимости между донорно-акцепторными свойствами а- и Яэлектронов, позволяет устранить некоторые из этих трудностей. Предположим, что данная группа L обладает свободными я-орби-талями, способными акцептировать электроны. Заполнение этих * Некоторые опыты [456] показывают, что в результате транс-влияния связь с лигандом А может ослабляться, но может и усиливаться. Предполагается, что последний случай реализуется, когда образование я-связей с транс-лнганлом А не играет существенной роли, а оттягивание электронного облака уменьшает электростатическое отталкивание лиганда А от центрального атома. Рис. IX. 3. Иллюстрация к а - я-теории трансвлияния. орбиталей приведет к повышению отрицательного заряда на L, который в отсутствие другого компенсируюшего процесса будет уменьшать акцепторные свойства этой группы. Таким компенсирующим механизмом может служить отдача а-электронов, которая увеличивается при увеличении отрицательного заряда на L. Другими словами, чем выше донорные свойства а-электронов группы L, тем выше ее акцепторные свойства для я-электронов, и, наоборот, акцептирование я-электронов повышает донорные свойства а-электронов. Это качественно вполне понятное явление может найти подтверждение и в количественном расчете (ср. с зависимостью энергии ионизации валентного состояния, определяющей смещение электронного облака при самосогласовании, от заряда на атомах, стр. 154). Таким образом, в том случае, когда лиганды не обладают в свободном состоянии существенными я-акцепторными свойствами, они могут появиться (усиливаться) в результате образования связи за счет повышенных а-донорных свойств. Тем самым получает качественное объяснение отмеченная выше связь между транс-активностью и восстановительными свойствами. Естественно вытекает отсюда и отмеченная И. И. Черняевым и А. Д. Гельман [460] корреляция между транс-активностью и ковалентностью связей, а также роль иенасыщенности лигандов [461]. Учет взаимозависимости я-акцепторных и о-донорных свойств, с включением в рассмотрение наряду с я-орбиталями и а-орбита-лей, позволяет дать некоторое качественное толкование и цис-влиянию [462]. Рассмотрим для наглядности плоско-квадратный комплекс Tpanc-PtLABj. Скорость реакции транс-замещения на координате L-Pt-А согласно сказанному зависит прежде всего от транс-активности лиганда L, т. е. от баланса его я-акцепторных и а-донорных свойств. Последние, однако, существенно зависят также от донорных свойств цис-групп В. Действительно, при смещении 0-заряда от цис-групп к центральному атому последний частично нейтрализуется и, соответственно, теряет способность принять а-заряд от лиганда L, вследствие чего его транс-активность падает. Но повышенные а-донорные свойства в координированном состоянии определяют и повышенные я-акцепторные свойства, и наоборот (вследствие их взаимозависимости). Отсюда следует, что чем выше транс-активность цис-групп В, тем меньше транс-влияние на координате L-Pt-А и, следовательно, скорость реакции трансзамещения. Иначе говоря, чем больше транс-активность данной группы, тем меньше ее цис-влияние, и наоборот. Сравним этот вывод с Э1у;периментальными данными по кинетике реакций замещения в плоско-квадратных комплексах [451]. Согласно сказанному, при замене хлора в комплексе PtCl4~ на аммиак скорость реакции замещения на координате С1-Pt-С1 должна увеличиваться, так как у аммиака транс-влияние меньше и, следовательно, цис-влияние больше, чем у Ch. Опытные данные подтверждают этот вывод: константа скорости реакции в рассмат- риваемом случае увеличивается в 2,7 раза. При аналогичной замене Вг- на NHs в комплексе PtBr4~ константа скорости реакции, согласно опытным данным, увеличивается в шесть раз, что также находится в согласии с теорией. Действительно, разность транс-активностей Вг и NHs больше, чем С1- и NHs, так что замена Вг на NH3 приводит к большему увеличению цис-влияния, чем при замене CI на NH3. Поэтому здесь следует ожидать большего увеличения скорости реакции, чем в случае хлоридных комплексов. Столь же естественно получают качественное объяснение и другие данные по цис-влиянию, приведенные в работах А. А. Гринберга с сотрудниками [451]. Таким образом, здесь замечается известная антибатность между транс- и цис-влиянием, качественно объяснимая о - я-взаимодей-ствием орбиталей. В этой схеме можно совершенно аналогично рассматривать и асимметрию в распределении плотности электронного облака в октаэдрических комплексах [458]. При этом любопытно, что низкая транс-активность группы NO2 в октаэдрических комплексах Pt (IV) [в отличие от ее высокой активности в плоских комплексах Pt (II)], явившаяся предметом обсуждения в некоторых работах [463], нашла естественное объяснение в предположении, что в октаэдрических комплексах группа NO2 по стерическим причинам расположена -под углами О < а < 90° к осям октаэдра и поэтому не может образовать я-связей с платиной [458]. Это предположение получило экспериментальное подтверждение в рентгено-структурном исследовании соединения 4 c-K2[Pt (N02)3013] [464]. И, наконец, усиление а - я-взаимодействия транс-активного лиганда с ц. а., вполне очевидно, ослабляет энергию связи транспартнера, доводя ее до чисто ионной (если она без учета трансвлияния является частично ковалентной*), результат, который получается и в электростатической поляризационной теории и который объясняет рентгеноструктурные данные Г. Б. Бокия с сотрудниками [465] об удлинении связи металл-лиганд из-за транс-влияния. Связь транс-активности с внутренним окислительно-восстановительным переносом заряда рассмотрена Гажо [466]. Дальнейшее развитие анализа электронного строения координационных соединений в аспекте их реакционной способности продолжено Лэнгфордом и Грэем [454]. Ими уделено еще большее внимание а-орбиталям с учетом понижения энергии промежуточного активированного комплекса (который предполагается пятикоординированной треугольной бипирамидой) за счет использования большего числа (двух вместо одной ра-орбиталей ц. а., передающих влияние по транс-координате. Необходимо подчеркнуть, что так как все изложенные представления сугубо качественны, приближенны, получаемые на их основе выводы не носят абсолютного характера. Поэтому не См. замечание па стр. 311.
|