
 |
|
|
Главная -> Природные воды свободного газа в виде микропузырьков, так как процесс удаления газа только посредством диффузии идет значительно медленнее вследствие малости коэффициента диффузии молекул газа в воде. При этом удается выделить до 95-98 % растворенного газа, а для удаления оставшегося требуется значительное время. Схема экспериментальной установки приведена на рис. 2.22. Методика эксперимента сводилась к следующему. Природная вода (Владивостокского городского водопровода) заливалась в емкость, соединенную с хлоркальциевой трубкой. Затем через маг- 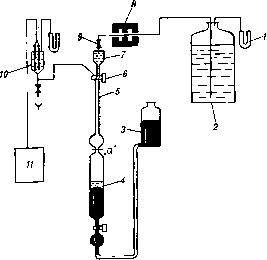 Рис 2.22. Схема эксперимента по определению кинетики удаления газа из природных вод при МГДА ПВ. / - хлоркальциевая трубка; 2 - водопроводная вода; 3 - уравнительный ссуд; 4 - прибор для вакууми-ровасния с ртутью; 5 - измеритель- Ная бюретка; 6 - кран; 7-воронка; в -магнитный аппарат; 9 - вентиль; /О - измерительная ячейка; - рН-метр. нитный аппарат, представляющий собой трехполюсной разнопо-лярный постоянный магнит, вода подавалась через вентиль, воронку, кран в измерительную бюретку и прибор для вакуумиро-вания. Причем отбиралась строго определенная порция 29,5 мл при температуре 20 °С путем опускания уровня ртути до отметки а . После этого кран закрывался и дальнейшим опусканием уровня ртути с помощью уравнительного сосуда создавался вакуум. В результате раствор вскипал и выделялся газ. Затем уровень ртути поднимался и производилось измерение объема выделившегося газа. Вакуумирование повторялось О раз и каждый раз производился отсчет объема выделившегося газа. После этого раствор подавался через кран в измерительную ячейку, где измерялось рН с помощью рН-метра (рН-30). Время проведения опыта 5 мин. Для сравнения контрольная проба воды пропускалась с той же скоростью, но при выключенном магнитном аппарате и все операции проводились по той же схеме. Во всех случаях процесс дегазации воды, прошедшей магнитный аппарат, ускорялся (рис. 2.23). Причем наибольший эффект для данной воды наблю- дался при Я = 2,1-10* А/м и скорости жидкости У=1 м/с. Число Re = 7500. Скорость воды в опыте варьировали от 0,3 до 1,5 м/с путем подбора стеклянных трубок различного диаметра в зазоре магнита. Заметное изменение скорости дегазации наблюдалось лишь при Re>5000. Причем статистический анализ экспериментальных данных, полученных в течение двух лет, свидетельствует о снижении, а порой и исчезновении этих изменений в весенний период. Полученные результаты (увеличение свободного газа на 25- 30 %) хорошо согласуются с приведенными выше представлениями Wm Пвг- Рис. 2.23. Количество газа, выделяемого из воды при ва-куумировании W=\(n). 1) Н=0; 2) H=3-W А/м, Re=7-i№; п - кратность вакуумирования. 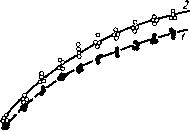 J I. I I I I I I В Юп О необходимости турбулизации потока и наличии свободного и растворенного газа в жидкости. Увеличение свободного газа в природной воде было экспериментально отмечено и в опытах [70] по флотации пульпы также с использованием метода вакуумирования. Экспериментальные исследования по кристаллизации растворов. В природных водах при кристаллизации труднорастворимых веществ, таких, как СаСОз, CaS04 и др., вследствие их низкой объемной концентрации образуются частицы весьма малых размеров, значительная часть которых находится за пределами разрешения оптического микроскопа. В частности, кристаллизация солей жесткости из слабых водных растворов, где объемная доля растворенного вещества 10--10-, сопровождается образованием кристаллов размером порядка нескольких мкм и меньше. Разработанным в лаборатории электромагнитных явлений Пензенского пединститута [69, 97, 98] методом проточной ультрамикроскопии изучалось действие магнитных полей на размеры микрочастиц кальцита и их число в единице объема раствора. Изучались частицы СаСОз размерами 0,1--2 мкм с помощью ультрамикроскопов ВДК-3, ВДК-4 и специальных приставок для измерения размеров частиц. Исследования проводились в прозрачной термостатированной плоской кювете. После прохождения жидкости через стеклянную трубку, помещенную в магнитное поле, она без доступа воздуха вводилась в кювету. В опытах использовали электро- магниты (B = 0,01-i-0,2 Тл). Эксперименты проводились с природными водами различного состава и с дистиллированной водой, куда вводилась затравочная суспензия кальцита. В отличие от обычно используемого кристаллохимического метода, когда исследуются размеры и число кристаллов после нагрева воды до кипения и выпаривания, этот метод позволяет вести прямое наблюдение и измерение микрокристаллов в процессе их роста, т. е. изучать кинетику процесса кристаллизации непосредственно. Исследования выполнялись как при комнатной температуре, так и в жидкости, нагретой до 85 °С, и при различном содержании N-IO%acmuu,/ai - ) 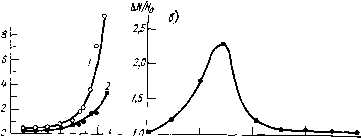 W 80t°C О 0,05 0,1 0,15 ВТл Рис. 2.24. Зависимость числа ядер кристаллизации СаСОз от температуры (а) N{t) при В=0 (/) и В=0,075 Тл (2) [97] и относительное изменение числа центров кристаллизации от индукции магнитного поля AN/No=f(B) при /°=const (б) [98]. углекислоты в растворах. Так как нижний предел измерения составлял 0,1 мкм, то уменьшение числа частиц в поле зрения микроскопа свидетельствует о растворении их, а увеличение - об их росте. При нагреве от О до 70 °С воды, содержащей карбонаты, вследствие понижения растворимости СаСОз с температурой раствор становится пересыщенным и концентрация частиц в нем увеличивается в 15-20 раз (рис. 2.24 а). Были проведены опыты с водопроводной водой (содержание свободной углекислоты 3 мг/л), и с водой, содержащей 100 мг/л углекислоты. Подсчет числа частиц показал, что при избытке углекислоты концентрация частиц уменьшалась на два порядка. Это свидетельствует о том, что подавляющее большинство видимых под микроскопом частиц следует отнести к ядрам кристаллизации карбонатной природы. При определенном значении В при V=l м/с, зависимость проходит через максимум (рис. 2.24). Скорость роста частиц СаСОз определяется концентрацией углекислоты в воде, причем эта зависимость при ВфО [98] изменяется. Для самых различных лабораторных экспериментов по кристаллизации СаСОз из растворов имеет место постоянство произведения УЯ (7-8) 10* А/С.
|